
病毒载体广泛应用于细胞治疗、基因治疗、病毒疫苗三大领域,用于将目的基因携带进入靶细胞从而实现对基因的修饰作用,表达目的蛋白,以治愈疾病。[1] GE生命科学-病毒载体工艺开发-谈具体参数?No!我们谈思路!
2.1工艺简介
2.1.1包装系统
目前常用的慢病毒(LV:Lentivirus)工艺开发采用四质粒系统(第三代包装系统),相比于第二代的三质粒系统,病毒的安全性进一步提升,减少重组成复制型病毒(RCV) 的可能性。
四质粒分别的作用:
- 一个具有目的基因的慢病毒表达质粒。表达质粒包含了包装、转染、稳定整合所需要的遗传信息。目的基因两侧各有一个LTR(long terminal repeat)序列,LTR序列促使目的基因整合到目的细胞基因组里。为了提高安全性能,表达质粒的3’LTR缺失了部分序列,使得整合后的病毒基因组失去自我复制能力。
- 两个包装质粒。其中一个质粒编码Rev,另外一个质粒编码Gag和Pol。
- 一个编码包膜蛋白的质粒。
- 将上述4个质粒共转染细胞。转染用的细胞常用293表达系统,且常采用瞬转工艺。区别于稳转工艺,瞬转系统在每次生产病毒时都需要重新进行病毒的包装,不会对已经感染病毒的293细胞建库。
2.1.2病毒生产方式
当前有两种广泛使用的首选病毒载体生产方式。多数研究者采用瞬时转染,或者在哺乳动物或昆虫细胞中获得稳定的生产细胞系。
大部分瞬时转染载体的生产使用贴壁依赖性细胞系,其中所选细胞类型需要有利于它们附着、生长和生产病毒载体的表面。
另一方面,稳定生产的细胞系通常是适应悬浮的细胞系,不需要基质附着、生长和生产病毒载体。
这两种病毒载体生产方式各有优缺点。因此,需要在临床开发的早期就要确定目标剂量和患者群体,以指导选择最优载体生产平台,从而满足未来的商业化需求。。[2] 病毒载体生产的上游生物工艺
2.1.2.1瞬时转染载体
瞬时转染载体优点:
- 瞬时转染涉及将遗传物质插入细胞中,而不需要将遗传物质整合到宿主细胞基因组中,该过程在操作上相对简单和直接。它还受益于以下因素:转染的遗传物质在细胞内停留的时间有限,并且不会转移至其他新的分裂细胞中。采用该工艺生产的病毒载体在转染后较短时间内就可以从细胞中收获。
- 与稳定的生产细胞系相比,基于瞬时转染的病毒生产相关的工艺开发时间相对较短。生物制药行业已经有多家成熟的供应商,拥有高效瞬时转染类载体生产需要的各种工具。但是,使用稳定的生产细胞系的载体生产方法还相对较新,并且正在进行支持行业不断增长的需求的工作。
- 瞬时转染是一种非常灵活和高效的病毒载体生产方法,它可以缩短开发时间并加速上市时间。
瞬时转染载体缺点:
它需要昂贵的GMP级质粒用于转染步骤,以及用于清除辅助质粒、细胞DNA和转染试剂的其他纯化步骤。
2.1.2.2 稳转细胞系
稳转细胞系经过基因修饰,通过诱导型启动子表达辅助基因、包装基因以及目标基因,用于生产病毒载体。稳转细胞系可以通过避免多质粒转染步骤简化病毒载体生产步骤,通过避免使用昂贵的cGMP质粒降低成本,通过生成历史清晰的细胞系最大程度地降低管控要求。
当前已获批或处于临床阶段后期的基因疗法,主要聚焦于治疗罕见的遗传疾病,其中目标患者人群数和每剂量的病毒颗粒的需求量相对较小。但是,老年痴呆症、帕金森症、类风湿性关节炎和血友病等疾病治疗的商业化面临巨大生产挑战,这是因为每剂量的病毒颗粒数会显著增加(对数级),并且患者人数也会更多。治疗此类疾病需要更多的病毒剂量和更高的病毒滴度,预计稳转细胞系的开发会显著提高病毒载体生产能力,满足这些疗法所需要的条件和规格。
稳转细胞系的开发可能需要较长的时间,这会增加上市时间。但是,一旦该细胞系经过工程改造和克隆可以达到更高的细胞密度和病毒载体滴度,该工艺最终会实现更高的生产效率并具备可扩展性。
许多公司正在积极开发设计人源细胞系,使其适合在悬浮培养的无血清培养基中生长。希望向稳定的人源生产细胞系的转变将减少管控安全问题,并通过提供糖基化修饰方式提高病毒载体在人体内的稳定性。
[3] 用于病毒载体生产的上游生物工艺(第2部分)
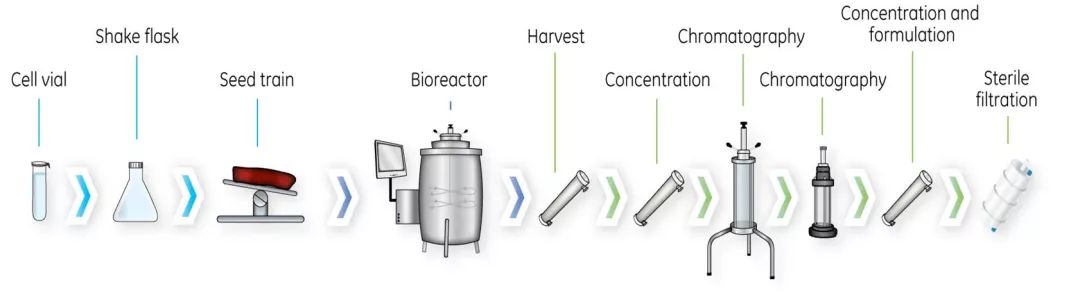
2.2工艺流程
病毒载体的生产工艺包括上游+下游两个部分。其中上游工艺的主要目的是为了得到一定滴度的病毒料液,而下游的主要目的是为了得到高滴度+高纯度的病毒载体来保证载体的效率和安全性。
[4] GE生命科学-病毒载体工艺开发-谈具体参数?No!我们谈思路
注:
根据病毒在细胞中的定位不同,习惯上可以将病毒载体大致分为裂解型病毒(如 LV 等)和非裂解型病毒(如 AAV、AdV 等)。
裂解型病毒包装完成后自行裂解细胞,释放到培养基中,收获含有病毒载体的细胞培养液即开始进行下游纯化;而非裂解型的病毒在进行下游纯化之前需要先进行细胞裂解,常用的技术为:反复冻融法和去垢剂法。
收获后的含有病毒载体的料液在进行层析或者超滤之前,一般都会经历核酸酶处理的步骤来降解大分子核酸物质,此过程的关键参数包括核酸酶浓度、反应温度、反应时间等。
2.3病毒的检测
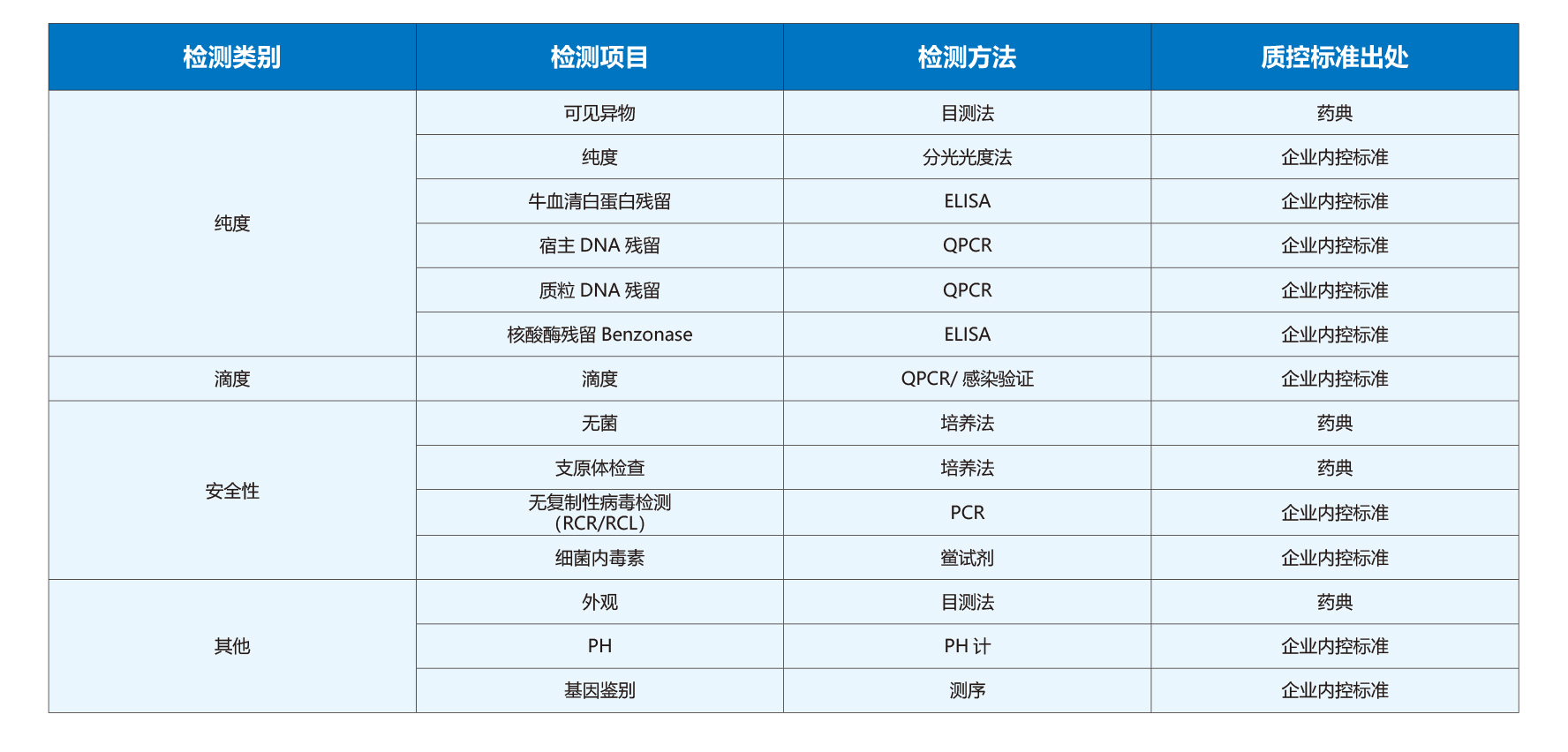
2.3.1 纯度杂质
1) 总蛋白
2)牛血清白蛋白检测
3)Benzonase-工艺开发过程酶切残留
4)宿主蛋白残留
5)宿主DNA残留
6)残留质粒
7)SV40
8) E1A
2.3.2滴度
1)感染滴度
2)病毒总颗粒
2.3.3安全性
1)无菌检测
2)细胞内毒素
3)支原体
4)RCL(具有复制能力的慢病毒ReplicationCompetentLentivirus)
2.3.4其他检测
1)pH值
2)外观
TBC


